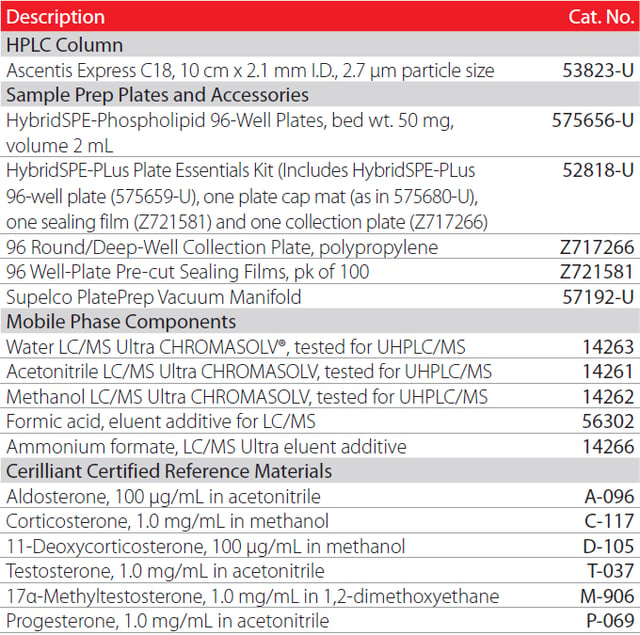
アフラトキシン類は、Aspergillus 属の真菌によって産生されるカビ 毒の一種です。アフラトキシン産生菌のうち、Aspergillus flavus と Aspergillus parasiticus は農業と医学における重要性から広く研究さ れています1。これらの種は、トウモロコシなどの穀物や落花生、ナッ ツ等の作物に感染し、作物がアフラトキシン類で汚染されることに より、人間や動物が日常的に摂取する食品にもたらされる可能性が あります2,3。これらの毒素は動物および人間が摂取すると、健康に 影響を及ぼす可能性があります4,5。アフラトキシン類は国際がん研 究機関(IARC)によって、グ ープ1 発がん物質、つまり、ヒトに発 がん性があることがわかっている化合物に分類されました6。その 標的は肝臓で、そこでDNA を変異させ、複製を阻害すると考えられ ます7。最も生物活性の高いアフラトキシンは、アフラトキシンB1(AFB1)です4。リスクアセスメントによれば、アフラトキシン類は世 界中で肝臓がん(HCC)の4.6 ~ 28.2% に関係する可能性があると 評価されました8。
本研究の焦点は、AFB1 の代謝物であるアフラトキシンM1(AFM1)です。AFM1 は、アフラトキシンに汚染された飼料を摂取した酪農動 物が泌乳するミルクに存在する可能性があります3。このアフラトキシンはその前駆物質より生物活性が低いにもかかわらず、IARC にグ ループ1 のヒトの発がん物質として分類されています6。アフラトキ シン毒性のある解釈によれば、「……それ以下では腫瘍形成が起こ らないという閾値濃度はないと通常思われます。……ゼロレベルの 曝露のみがリスクゼロとなります……」9。AFM1 は、発がん物質とし ての可能性こと、および牛乳が特に子供と幼児の食物源として広く 使われていることから乳中の濃度は規制されています10。
欧州連合(EU)は、イスラエルとともに、生乳および乳を原材料とす る食品の原料乳でのAFM1 の存在量について、非常に厳しい上限を 課しました。現在、EU およびイスラエルの乳製品におけるAFM1 の 許容限度は、0.050 μg/kg であるであるのに対し、幼児の粉ミルク、 フォローアップミルクおよびその他の乳幼児向け栄養食品における AFM1 の規制値は、0.025 μg/kg です11,12。
これをLC/MS で分析できるかどうかを、乳サンプルをタンパク質 沈殿しFLD を用いて調べました。サンプルにAFM1を0.5ng/mL(0.5 μg/kg)で添加し、HPLC で分析したところ、回収率は88%と充分な クリーンアップでAFM1 を検出できることがわかりました。本研究 をさらに進め、世界で最も低濃度であるEU の規制値でアフラトキ シンM1 を検出定量できるよう、AFM1 サンプルのクリーンアップ法 および分析法を開発します。方法がうまくいけば、米国および中国 が定めた牛乳中AFM1 の規制限度の分析が可能になるでしょう13,14。
実験
乳の調製
脂肪分2%の乳45 グラムを、ポリプロピレン製の遠心分離用試験 管(50mL)* に入れ、5000 rpm、相対遠心力(RCF)4863 x g** で60 分間、遠心分離しました。遠心分離後、0°C で30 分間冷却し、上部 (脂肪)層をスパチュラで除去した後、20mL の乳清(中層)をフラスコに移しました。
アフラトキシンの添加
0.5 μg/mL のAFM1 標準物質150 μL を、1350 μL のアセトニトリル で希釈し、0.05ug/mL に調製しました。シラン処理した三角フラス コ(200mL)* 2 個にそれぞれ調整した乳を80mL ずつ入れ、0.05ug/ mL に調製したAFM1 溶液を40 および400 μL 添加し、AFM1 の濃 度を25 および250 pg/mL としました。乳へのAFM1 の添加後、2 分間穏やかに撹拌し抽出に供しました。
タンパク質沈殿およびAFM1 の抽出
アセトニトリルを20mL をポリプロピレン遠心分離管(50mL)に入 れ、AFM1 を添加した乳を5 mL 加え、タンパク質を沈殿させました。 この混合物を手動で5 秒間振盪し、Supel QuE non-buffered tube2(カタログ番号55295-U)を1 本加え、塩類を分散させるため、すぐ にその懸濁液を激しく振盪しました。その後、その遠心管を実験室 用振盪機で5 分間振盪を行い、振盪後、試験管を20 分間 5000rpm (RCF 4863 x g)で遠心分離しました。AFM1 は、調製物の有機層(上 部)に抽出されました(図1a)。

サンプルのクリーンアップ
Supel™ Tox AflaZea SPE カートリッジ(カタログ番号55314-U)を、 16 × 125 mm のシラン処理をしたガラスの捕集管を置いたラック 付きバキュームマニホールドに装着しました。真空を-5" Hg に設定 し、各抽出物の上部層からのサンプルを10.0 mL、SPE カートリッジ にロードし、カートリッジ内にサンプルが残らないよう押し流すため に、サンプル溶液が溶出した後すぐに100% のアセトニトリルを 2mL × 2 回流しました。
サンプルの蒸発、再溶解および分析
精製したサンプルを、10 psi の窒素流下、70°C で蒸発させました。 窒素流は、3 psi で開始し、5 分ごとに6 psi、最終的には9 psi まで増 加させました。乾燥残査にアセトニトリル:水(20:80)の500 μL を ピペットで加えることによってサンプルを再溶解し、続いて30 秒間 ボルテックスで混合しました。次いで、溶解した残査を、パスツール ピペットで、ポリフッ化ビニリデン(PVDF)フィルター(13 mm/0.2 μm)が先端に付いた1 mL のシリンジに移し、750 μL のポリプロピ レンバイアルに入れました。抽出濃度12.5 pg/mL ~ 500 pg/mL(絶 対濃度250 pg/mL ~ 10,000 pg/mL)のマトリックスマッチング校 正用スタンダードを使って定量を行いました。
結果および考察
最初に乳を遠心分離して、脂肪と無脂乳固形物(NFMS)を除去しま した。n = 16 で、重量平均で乳の2.6% の脂肪および0.7% のNFMS を除去しました。
Supel Tox AflaZea SPE カートリッジを使用したサンプルクリーン アップは、簡単で迅速に行うことができました(1 分未満/サンプル 数n = 3)。SPEクリーンアップにより、アフラトキシンM1は溶出され、 乳に含まれる望ましくない妨害物は、カートリッジに保持されまし た。他のSPE 方法では、対象の分析対象物がカートリッジと結合し て、様々な洗浄ステップの後に溶出されるのですが、それと比較す るとこの前処理手順は必要なステップがより少なく、サンプル調製 時間を短縮できます。また、蒸発時間は約30 分でした。
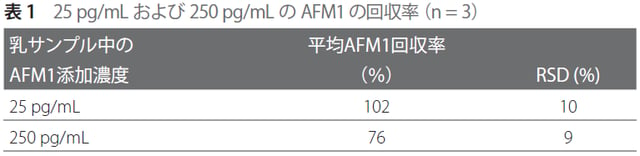
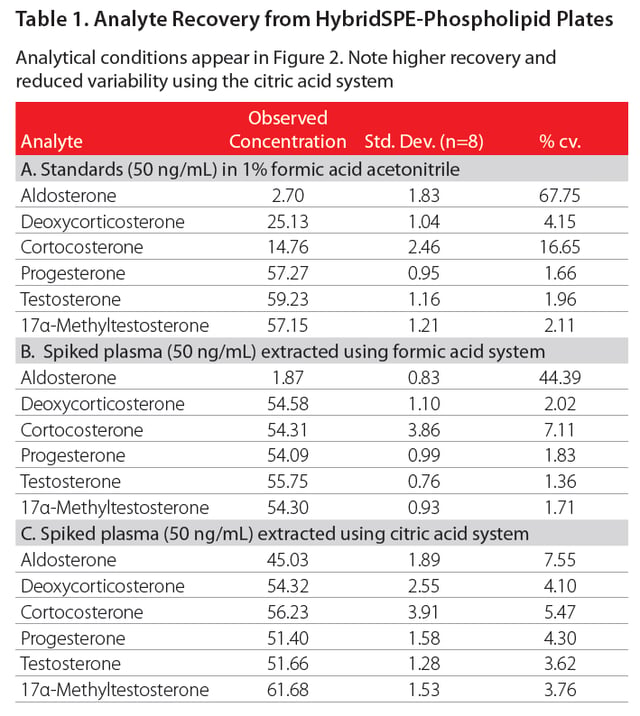
図1b に見られるように、AflaZea 精製サンプルは、残査およびサン プルの色合いという点で未精製サンプルよりもきれいに見えまし た。図2 のクロマトグラムから、AFM1のピークはどちらの濃度でも、 マトリックス干渉もなく、バックグラウンドからの識別が容易である ことがわかります。また表1 から、25 pg および250 pg のどちらの 濃度でもAFM1 は、許容できる回収率(それぞれ102% および76%) ならびに、優れた再現性(それぞれ10.2% RSD および8.6% RSD)で 検出され、定量されたことがわかりました。したがってこのSPE 法 は、25 pg/mL および250 pg/mL のどちらの濃度の乳でもAFM1 の 定性と定量のために十分なサンプルクリーンアップができることが 立証されました。
結論
乳サンプル中のアフラトキシンM1 を、EU 規制基準(0.025 μg/kg) に対応するよう迅速にクリーンアップ、分析および定量する方法を、 Supel™ Tox AflaZea SPE およびLC/MS 分析を使って開発しました。 他のSPE 法でよくみられる、手順が多く煩雑になってしまう前処理 (保持および溶出)とは異なり、Supel Tox AflaZea では「妨害物除去」 操作を用い、洗浄ステップをなくして時間を短縮しました。このSPE 法は、乳および乳製品で問題となるマトリックス干渉をタイムリー に除去するのに役立ちました。その一方で分析対象物の高い回収率 および優れた再現性も達成しました。また予備実験を行ったところ、 さらに高濃度のAFM1 サンプルを扱う場合、このサンプル調製方法 をHPLC、FLD 法にも適用できることがわかりました。
References
1. NC State University Carbone Lab Site. http://carbonelab.org/aspergillus (accessed Jan 2014)
2. Cornell University College of Agriculture and Life Sciences Site. http://www.ansci.cornell.edu/plants/toxicagents/aflatoxin/aflatoxin.html (accessed Jan 2014)
3. University of Arkansas Division of Agriculture Site. http://www.uaex.edu/Other_Areas/publications/PDF/FSA-4018.pdf (accessed Jan 2014)
4. U. S. Food and Drug Administration Foodborne Illness and Contaminants
Site. http://www.fda.gov/Food/FoodborneIllnessContaminants/CausesOfIllnessBadBugBook/ucm071020.htm (accessed Jan 2014)
5. Robens, J.F.; Richard, J.L. Aflatoxins in animal and human health. Rev Environ Contam Toxicol. 1992, 127, 69-94.
6. International Agency for Research on Cancer: IARC Monographs on the Evaluation of Carcinogenic Risks to Humans Site. http://monographs.iarc.fr/ENG/Classification/ (accessed Jan 2014)
7. International Agency for Research on Cancer: IARC Monographs 100-F Site on Aflatoxins. http://monographs.iarc.fr/ENG/Monographs/vol100F/mono100F-23.pdf (accessed Jan 2014)
8. Liu, Y.; Wu, F. Global Burden of Aflatoxin-Induced Hepatocellular Carcinoma: A Risk Assessment. Environ Health Perspect. 2010, 118, 818–824.
9. Codex Committee on Food Additives and Contaminants Archive Site. http://ec.europa.eu/food/fs/ifsi/eupositions/ccfac/archives/ccfac-cx-16a-ec-comments-130300final_en.pdf (accessed Jan 2014)
10. Anfossi, L.; Baggiani, C.; Giovannoli, C.; Giraudi, G. Occurrence of Aflatoxin M1 in Dairy Products, Aflatoxins – Detection, measurement, and Control, Dr Irineo Torres-Pacheco (Ed.), 2011, ISBN: 978-953-307-711-6, InTech, Available from: http://www.intechopen.com/books/aflatoxins-detection-measurement-andcontrol/occurrence-of-aflatoxin-m1-in-dairy-products
11. Commission Regulation (EU) No 165/2010. Amending Regulation (EC) No 1881/2006 Setting Maximum Levels for Certain Contaminants in Foodstuffs as Regards Aflatoxins. Official Journal of the European Union, Feb 26, 2010, pp L 50/8 – L 50/12.
12. Britzi, M.; Friedman, F.; Miron, J.; Solomon, R.; Cuneah, O.; Shimshoni, J. A.; Soback, S.; Ashkenazi, R.; Armer, S.; Shlosberg, A. Carry-Over of Aflatoxin B1 to Aflatoxin M1 in High Yielding Israeli Cows in Mid- and Late-Lactation. Toxins,
2013, 5, 73-83.
13. U. S. Food and Drug Administration: Inspections, Compliance, Enforcement, and Criminal Investigations. http://www.fda.gov/ICECI/ComplianceManuals/CompliancePolicyGuidanceManual/ucm074482.htm (accessed Jan 2014)
14. Liang, J.; Song, X.; Zhu, J.; Li, N.; Xu, H.; Li, F. Suitability Analysis of Tolerance Limit for Aflatoxin M1 in Foods and Chinese Population Dietary Exposure to Aflatoxin M1 From Milk. Wei Sheng Yan Jiu. 2013, 42, 840-843.