読者からのHPLC分析法に関する質問に答えたり、Journal of Chromatography誌への投稿論文を審査している時に、私は、喜ぶべきか、あるいはがっかりするべきか、分からなくなることがあります。HPLC分析法が、いったいどれくらいの頻度で、私がgenetic driftと呼んでいる変化を受けてきたのか、驚きを感じます。現在のHPLC分析法は、新しい問題を解決するために、それ以前の分析法を、ずっと微調整してきた結果、出来上がってきたからです。今回は、その一例について紹介します。
C18カラムを用いて、流速が1.0mL/分、移動相として、65%メタノール(MeOH)および25mMのリン酸塩と25mMのトリエチルアミン(TEA)をリン酸でpH2.5に調整した緩衝液を35%混合した溶液を使用するHPLC分析法について考えます。一見、とてもシンプルな分析法のように感じませんか?しかし、何のためにTEAが加えられているのでしょう?TEAはµBondapak、Novapak、Lichrosorb、Supelcosil、Zorbax、Hypersilなどの1990年より以前に一般的に使われていた、古いタイプで純度が低いType-Aシリカカラムが一般的だった頃には、一般的な移動相添加物でした。これらのカラムには、不純物として多くの金属が含まれていた上に、特に塩基性化合物に対してひどいピークテーリングを引き起こす強酸性のシラノール基が存在するシリカ粒子が充填されていました。このピークテーリングを和らげる一つの方法が、移動相に低分子量の塩基を加える方法でした。この塩基は、シリカ上に存在する酸性の活性部位に対して、塩基性試料と競合するため、移動相に一定濃度を加えることにより、テーリングを抑えることができます。この方法には意味があり、何年もの間、何千ものHPLC分析において、移動相に塩基を加えることが賢明であると考えられてきました。しかし、1990年代の中頃に、新しく、高純度のType Bシリカが登場することにより、古いタイプのシリカは多くの場合において使用されなくなってきました。しかし、未だにTEAが使われているのは何故でしょうか?TEAは必要なのでしょうか?TEAが無いと、何か困るのでしょうか?その答えはおそらく、Noです。
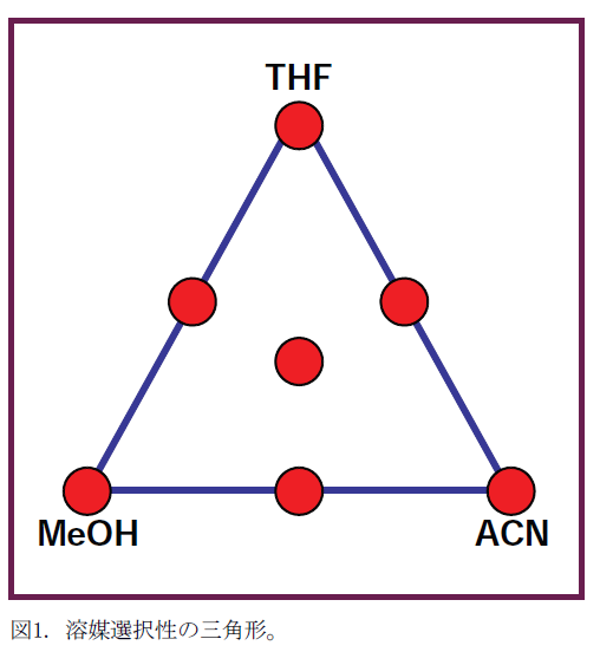
例えば、MeOH、アセトニトリル(ACN)および緩衝液の様に、2つ以上の有機溶媒を用いている方法はどうでしょうか。これも、一見、とてもシンプルな移動相ですが、この場合、何が間違いなのでしょうか?クロマトグラフィーの歴史を振り返ってみると、1970年代後半から1980年代前半にかけて、溶媒の選択性の利点を得ることに関し、大きな動きがありました。Lloyd Snyder氏、Jack Kirkland氏、Joe Glajch氏らの研究により、図1に示す様な、分析方法開発のための"solvent triangle"という考え方が提案されました。そして、当時、HPLCのビジネス展開をしていたDuPont社からSentinalという名前で市販され、その後、Perkin-Elmer社からPESOS (Perkin-Elmer Solvent Optimization System)という名で販売されました。この方法はアイソクラティック溶離で使用することができます。仮に、皆さんがMeOHを有機溶媒として用いた場合の最適な分離を達成するために、Me0H-緩衝液移動相を使ったとします。この場合には次に、ACN-緩衝液およびテトラヒドロフラン(THF)-緩衝液においても同様の分離を行ないます。これらの結果は、図1において、三角形の各頂点(図1の赤い点)を形成します。次に、各頂点の移動相を1:1で混合し、各辺の中点の移動相組成を、更に、各頂点の移動相を1:1:1で混合して三角形の中心の移動相組成を調製します。これら7点の測定結果から、クロマトグラムの見た目の比較あるいは、市販の計算プログラムを用いることにより、目的の分離に対して最適移動相溶媒を見つけることが可能です。
この方法は、クロマトグラフィーに関する知識が乏しかった当時は画期的なアイデアでしたが、多くの知識が蓄積されてきた今日となっては、このような複雑な方法は、もう必要ではありません。線形溶媒強度理論およびDryLabの様な分離モデルに関するソフトウェアの開発により、三成分あるいは四成分の移動相は、ほぼ必要ではなくなりました。私がこれまでに行ってきた、多くの分析について思い出してみると、本当に三つの溶媒が必要であった分析は、片手で数えられるくらいしかありません。もう現在では、三溶媒移動相の必要性は無いでしょう。
酸と塩基が混在する試料を分離するために、良く考えられた方法があります。その方法は、酸試料のイオン化を抑制して保持を改善するために、移動相中に低pHのバッファーを加えるとともに、塩基試料の保持を改善するために、イオン対試薬も加えます。この方法は非常に効果的です。もし、皆さんが酸試料を分析する方法の開発を行う必要がある場合は、この方法から始めてはいかがでしょうか?特に何かの役に立つ訳ではありませんが、この分析法はイオン対状態で分析が終了します。
図1. 溶媒選択性の三角形.
KISS
私はKISS (Keep It Simple, Stupid)(簡単・単純にしておこう)の原則を強く信じていますが、同僚の一人に、もっと政治的に正しく、かつScandinavian spelling(スカンジナビア語のスペル)を使って、KYSS (Keep Your Solvents Simple)(溶媒組成を単純にしなさい)と表現するように言われました。どちらにせよ、移動相に何かを加えることは、問題が起こる可能性を増やすだけです。以前の方法を元にして、新しい分析法を開発することは適切ですが、その際、元の分析法で使った各移動相成分について再確認する必要があります。何故その成分が含まれているのか?分離に何か役に立っているのか?その成分は問題の原因にはならないか?もし、その成分が含まれている理論的な理由があるのならば、是非そのままにしておいて下さい。しかし、その試薬がなぜそこに含まれているか分からない時は、そのままにしておくのか、よく考えて下さい。
分析法に関しては、genetic driftを受け入れてはなりません。ダーウィンの法則はクロマトグラフィーには適用するべきではないのです。分析法Aを分析法Bに変形させると、それは分析法Cに変化し、更に、その後分析法Dに変化します。分析法Dは分析法Aで対象としていたような種類の試料を分析することさえできませんが、依然として、分析法Aで行った分析のための特有の成分を含んでいます。適切にクロマトグラフィーの原理に基づいた分析法を構築すれば、予期せぬ変化が起こった時でも、あまり驚くことは無いはずです。


