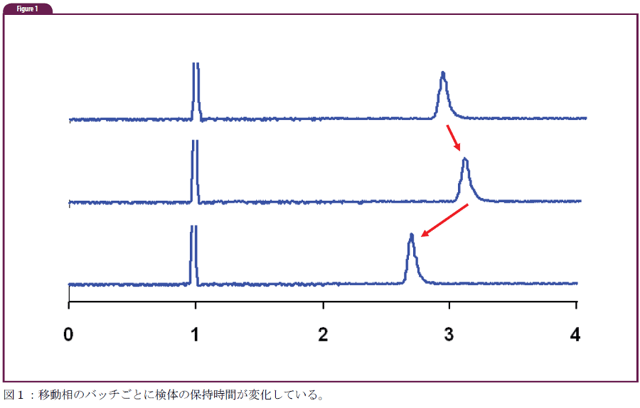
Q:HPLCの移動相の水性部分をpH 2.5に調整するためにトリフルオロ酢酸(TFA)を用いています。どんなに注意深くpH調整を行なっても,移動相の新しいバッチを準備するたびに保持時間に変化が見られるのです(図1参照)。一回のバッチ内では保持時間は一貫しているようですが,バッチごとに変動することが気になります。この問題を解明していただけませんか?
JWD:TFAはプロテインやペプチドなど生体分子のHPLC分離において,移動相の添加物としてよく用いられます。それはTFAが,イオン対試薬として働いてすぐに平衡状態に達するため,勾配溶出で用いることができるからです。標準的な調合としては,A溶媒に0.1%のTFAの水溶液を,B溶媒には0.1%のTFAのアセトニトリル(ACN)溶液を入れます。
TFAはまたその揮発性によって,LC-MSアプリケーションの添加物としてもよく用いられていました。しかし,現在ではほとんどの場合,ギ酸の方が選ばれているようです。これは,TFAが検体の分子のイオン化を抑制することが分かったからです。
TFAがこのように普通に用いられることは,TFAがあたかも,移動相の準備用のその他の酸と全く同じように用いることができるもののように考えて安心してしまうことがあります。でも気を緩めてはいけません。移動相のpHが,この質問者が行ったように酸の滴定で調整される時,一定のpHを得るために必要となる酸の総量は,酸のpKaと水のpHによって決定されるのです。もしpHが唯一の懸念であるなら,添加された酸の量の多少の違いはたいして重要なことではないでしょう。しかし,その酸が,他の特性でもクロマトグラフィ・システムに影響しているなら,量の違いは非常に重要なものになります。選択した標準物質によりますが,TFAのpKaはpH 0.2-0.5の範囲にあります。0.1%のTFAは,大体1.8-2.0のpHになります。つまりpH 2.5には,0.1%以下のTFAしか加えないということです。なお,TFAはイオン対試薬としても作用するということを覚えていてください。イオン対の保持時間は,イオン対試薬の濃度に対して非常に敏感になります。したがって,pHを2.5に調整するために必要なTFAの量がバッチごとに変わったのなら,それは水のpHが違ったためそこにあるイオン対試薬の量も違ったからだということが分るでしょう。質問者が観測した保持時間の変化の原因はここにあるのだと思います。
この仮説をどうやってテストすればよいのでしょうか? まず,pH 2.5を得るためにいつもどのくらいのTFAを添加するのかを算定します。これは,通常の方法でpH 2.5まで滴定することでなされますが,目盛り付きのビュレットか容積測定用のピペットを用いて,1-Lの水をpH 2.5にするにはどのくらいのTFAが必要かを測ります。次に,一連の3つの濃度のTFA-水溶液を作ります。1つは今作った溶液です。もう1つは0.1%のTFA溶液,3つ目はこの2つの中間濃度のものです。3つの溶液をそれぞれ流し込んでみて,検体の保持時間を測定してください。保持時間はTFAの濃度と相関することがわかると思います。この知識を基にすれば,要望通りの保持時間を得るための濃度を見つけ出すことができるでしょう。個別のpHの代わりに,このTFA濃度を移動相の標準的調整に用いれば,バッチごとの保持時間の再現性がより一貫したものになるはずです。
もしTFAがイオン対試薬として作用していない場合,そしてpH 2.5の移動相を得ることがより重要であるなら,他の酸を用いた方がいいかもしれません。私ならギ酸を試してみます。ギ酸0.1%で,目標のpH 2.5になるはずです。上述のTFAでの手順と同じように,酸を用いてpHの調整を試みるよりは,一定量の酸を用いる方が一貫した結果が得られるはずです。特定のpH値を得ることが必要だというのなら,バッファーの方がより良い選択になるでしょう。ジョン・ドランのHPLC Solutionの次回の記事に,バッファーの使用についてより多くの情報が掲載されますので,それをご覧ください。
図1:移動相のバッチごとに検体の保持時間が変化している。
エキスパートのための、無料学習!
無料のウェビナー、オンライントレーニング、トラブルシューティング、アプリケーション、テクニカル情報、そしてブログを受け取り、更に学びませんか。下記にEmailアドレスを記入し、サインアップしてください。


